| El movimiento browniano por María del Mar Moya Sánchez y María del Carmen Murcia Cano |
||
| En 1827 el botánico Robert Brown observó un movimiento accidentado de los granos de polen en una suspensión acuosa. En 1905, Einstein remitió un artículo a Annalen der Physik en el que desentrañaba la naturaleza molecular de este fenómeno. | ||
Cuando en una habitación oscura penetra un rayo de sol es frecuente observar partículas de polvo suspendidas en el aire en un continuo movimiento oscilante. Éstas partículas no solo no caen, sino que incluso, llegan a presentar un movimiento ascendente a pesar de ser más densas que el aire. Si en un vaso de agua ponemos con cuidado una gota de tinta veremos que poco a poco se va extendiendo por todo el volumen del agua con un movimiento aleatorio, dando lugar a formas caprichosas. Si repetimos el experimento, pero con agua caliente, observaremos que la tinta se difunde con mayor rapidez. ¿A qué se deben estos fenómenos? ¿Tienen algo en común?
El movimiento browniano fue descrito por en 1828 por el botánico inglés Robert Brown (1773-1858). Observó al microscopio que en una suspensión de polen de Clarkia pulchella en agua los granos tenían un movimiento muy accidentado, en zig-zag. Brown llegó a la conclusión de que estos movimientos no surgían de corrientes en el líquido que los contenía, sino que eran propios de la misma partícula. En un principio se sugirió la hipótesis de que el movimiento se pudiera deber a que el polen tuviese vida; esto se desechó al comprobar que tanto el polen de plantas que habían muerto muchos años antes como las partículas minerales en suspensión presentaba el mismo movimiento. Otras hipótesis apuntaban a que las fuerzas eléctricas empujaban a las partículas de un lado a otro, a la convección, la evaporación o la luz. Finalizó el siglo XIX sin una explicación convincente de la naturaleza de este fenómeno. En esa época aún era cuestionada la estructura atómica de la materia. En 1905 Albert Einstein publicó un trabajo en el que explicó el movimiento browniano. Hasta ese momento los argumentos propuesto para explicarlo habían sido cualitativos, no se había formulado ninguna hipótesis de la que se pudiera extraer una conclusión capaz de ser comprobada experimentalmente. Einstein contrastó las leyes de la termodinámica con la teoría cinética, basada en la suposición atómica. En particular se interesó por las conclusiones que se obtendrían si el movimiento browniano se tratara de explicar por medio de la hipótesis atómica.
Einstein señalo la relación que existía entre el movimiento y el calor y destacó que el calor se traduce en el movimiento aleatorio de las partículas. Einstein dedujo en su artículo parte de la teoría matemática que subyace al movimiento browniano. Cuanto más pequeña es una partícula más sensible es su movimiento respecto a las partículas del medio y más caótica es su trayectoria. Obtuvo predicciones cuantitativas que podían comprobarse con resultados experimentales. Concluyó que la segunda ley de la termodinámica únicamente se cumple en promedio y que el movimiento de las partículas está relacionado con la temperatura del fluido, con su viscosidad, con las dimensiones de las moléculas y con el número de Avogadro, número de átomos o moléculas que contiene un mol de una sustancia. En un principio este número se calculó en 6.4×1023. Hoy día se ha calculado con más exactitud 6.023×1023. Una de las aplicaciones más recientes del movimiento browniano es el diseño de filtros o cribas brownianos, que transforman el movimiento aleatorio de las partículas en un desplazamiento sistemático. Estos inventos aprovechan que las partículas en suspensión describen trayectoria caóticas para transformar mediante obstáculos asimétricos un movimiento aleatorio en uno sistemático. Mediante este sistema se pueden clasificar estructuras microscopicas como los virus según su tamaño. |
||

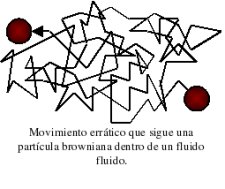 En ambos casos se trata de partículas en suspensión que se mueven dentro de un fluido. Este, recibe el nombre de movimiento browniano y se caracteriza por ser continuo y muy irregular. La trayectoria que seguiría una partícula dentro de un fluido se puede ver en la figura de la derecha.
En ambos casos se trata de partículas en suspensión que se mueven dentro de un fluido. Este, recibe el nombre de movimiento browniano y se caracteriza por ser continuo y muy irregular. La trayectoria que seguiría una partícula dentro de un fluido se puede ver en la figura de la derecha.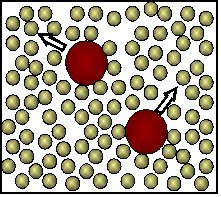 Einstein propuso que las partículas se mueven sin rumbo aparente en un líquido debido a que son bombardeadas por las moléculas del líquido desde todos los lados en un número sorprendentemente alto de choques, del orden de 1020 impactos en cada segundo. El efecto acumulado de tales colisiones resulta apreciable. El resultado es que la partícula suspendida experimenta un cambio de velocidad y de dirección. Los cambios son impredecibles tanto en magnitud como en dirección, ya que la magnitud de colisiones no permite seguir el efecto individual de cada una de ellas.
Einstein propuso que las partículas se mueven sin rumbo aparente en un líquido debido a que son bombardeadas por las moléculas del líquido desde todos los lados en un número sorprendentemente alto de choques, del orden de 1020 impactos en cada segundo. El efecto acumulado de tales colisiones resulta apreciable. El resultado es que la partícula suspendida experimenta un cambio de velocidad y de dirección. Los cambios son impredecibles tanto en magnitud como en dirección, ya que la magnitud de colisiones no permite seguir el efecto individual de cada una de ellas.